코오롱생명과학, 다음달 미국서 신경병증성 통증치료제 임상1상/2a상 시작
전세계 통증질환 시장의 8분의 1 차지, 2022년에 4조원
코오롱생명과학은 지난해 3월 미국 FDA에서 IND 승인된 신경병증성 통증치료제 신약(KLS-2031)의 미국 임상1상/2a상을 개시한다고 24일 밝혔다.
신경병증성 통증은 신경계 손상이나 기능 이상으로 발생하는 난치성 질환으로, 환자들에게 극심한 고통을 주는 감각신경계 질환이다. 해당 시장은 전세계 통증질환 시장의 8분의 1가량을 차지하며, 오는 2022년에 4조원의 규모가 형성될 것으로 예측되고 있다.
문제는 기존의 대부분 치료제는 진통제 계열인데 지속적인 효과가 이어지지 않으며, 최종 진통제로는 아편계열의 마약성 의약품이 사용돼 미충족 의료수요가 높다는 점이다.
KLS-2031은 기존 시판 치료제로 효과를 보지 못하는 신경병증성 통증환자들을 타겟으로, 1회 국소 주사시 진통 효능이 장기간 지속되도록 개발됐다.
이는 신경병증성 통증치료 방식과 다르게 특허 받은 유전자 조합을 이용하는 주사 요법 치료제다.
코오롱생명과학은 지난해 3월 미국 FDA로부터 IND 승인을 받았고 지난해말 미국 내 임상기관과의 IRB 첫 승인을 마치면서, 올해 3월부터 2개 임상기관에서 안전성 및 유효성 평가를 목적으로 한 임상 1상, 2a상이 진행될 예정이다.
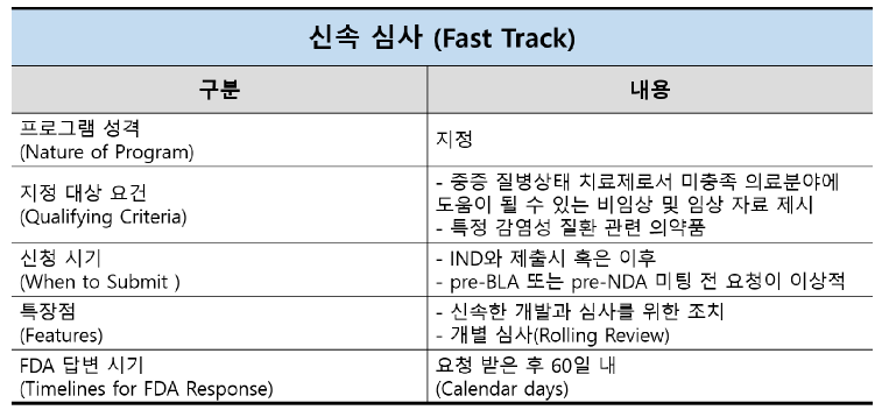
특히 이는 신경병증성 질환 중 요천골 통증에 대한 First-in-class 신약 후보물질로, 이번에 패스트트랙으로 지정돼 우선심사 등 기간 단축 혜택을 받아 출시 일정이 앞당겨질 전망이다.
코오롱 측은 "미국 FDA의 최근 3년간 총 153개 신약 승인 중 39%가 패스트트랙 지정 제품이었고, 65%(99개)는 우선심사를 거쳤다"며 "앞으로 개발 기간 단축과 임상 2, 3상의 빠른 설계와 검토도 가능해질 것"으로 내다봤다.
이어 "요천골 외에도 다른 신경병증성 통증질환까지 확장성을 가질 수 있는 신약으로 개발하겠다"면서 "글로벌 파트너사와의 협업과 밀접한 커뮤니케이션으로 근원적 치료제를 만드는 데 다양한 방향을 모색하겠다"고 강조했다.
신경병증성 통증은 신경계 손상이나 기능 이상으로 발생하는 난치성 질환으로, 환자들에게 극심한 고통을 주는 감각신경계 질환이다. 해당 시장은 전세계 통증질환 시장의 8분의 1가량을 차지하며, 오는 2022년에 4조원의 규모가 형성될 것으로 예측되고 있다.
문제는 기존의 대부분 치료제는 진통제 계열인데 지속적인 효과가 이어지지 않으며, 최종 진통제로는 아편계열의 마약성 의약품이 사용돼 미충족 의료수요가 높다는 점이다.
KLS-2031은 기존 시판 치료제로 효과를 보지 못하는 신경병증성 통증환자들을 타겟으로, 1회 국소 주사시 진통 효능이 장기간 지속되도록 개발됐다.
이는 신경병증성 통증치료 방식과 다르게 특허 받은 유전자 조합을 이용하는 주사 요법 치료제다.
코오롱생명과학은 지난해 3월 미국 FDA로부터 IND 승인을 받았고 지난해말 미국 내 임상기관과의 IRB 첫 승인을 마치면서, 올해 3월부터 2개 임상기관에서 안전성 및 유효성 평가를 목적으로 한 임상 1상, 2a상이 진행될 예정이다.
특히 이는 신경병증성 질환 중 요천골 통증에 대한 First-in-class 신약 후보물질로, 이번에 패스트트랙으로 지정돼 우선심사 등 기간 단축 혜택을 받아 출시 일정이 앞당겨질 전망이다.
코오롱 측은 "미국 FDA의 최근 3년간 총 153개 신약 승인 중 39%가 패스트트랙 지정 제품이었고, 65%(99개)는 우선심사를 거쳤다"며 "앞으로 개발 기간 단축과 임상 2, 3상의 빠른 설계와 검토도 가능해질 것"으로 내다봤다.
이어 "요천골 외에도 다른 신경병증성 통증질환까지 확장성을 가질 수 있는 신약으로 개발하겠다"면서 "글로벌 파트너사와의 협업과 밀접한 커뮤니케이션으로 근원적 치료제를 만드는 데 다양한 방향을 모색하겠다"고 강조했다.
저작권자© 메디게이트뉴스, 무단 전재 및 재배포 금지
서민지 기자 (mjseo@medigatenews.com)
전체 뉴스 순위
칼럼/MG툰
English News
- LOTTE BIOLOGICS Hosts Technology Development Forum to Foster Future Innovation
- Hanmi Highlights Next-Generation Obesity Pipelines at ObesityWeek 2025
- SK bioscience Earns 'A' Rating in KCGS ESG Assessment for Fourth Consecutive Year
- Huons N to Acquire Health Functional Food Manufacturer 'Biorosette'
- European Commission Grants Approval of Remsima IV Liquid Formulation, World's First Liquid Formulation of IV Infliximab
유튜브
사람들